特長 > チェイン間の距離関係を調べる
タンパク質間の距離関係を調べる Chain Interface
他のチェインとの距離関係を調べる
サブユニット間の相互作用や、蛋白質とDNAとの相互作用に関するアミノ酸残基を検出するには、Chain Interfaceが便利です。2つのChainの構造から指定した距離範囲にある残基を一括して抽出できます。抽出されたアミノ酸残基の構造はWorkspaceに出力され、インターフェイスブラウザでは表形式で確認できます。距離に応じて色分け表示により、他のチェインからの距離が一目で確認できます。
抽出された部分はWorkspaceに格納され、詳細を確認することができます。
全体構造での抽出部分
ダイマーインタフェースを検出する
Chain Interface機能を使用して、ダイマーインタフェースを検出することができます。ダイマー間の相互作用に関するアミノ酸残基を見つけるのに便利です。距離に応じて色分け表示すれば、アミノ酸配列上でも、もう一方のサブユニットに近いアミノ酸残基が確認できます。一方のサブユニットを非表示にすれば、接触面も見やすくなります。抽出された残基はWorkspaceに格納されます。抽出された残基だけを見て、相互作用する残基どうしを確認することができます。
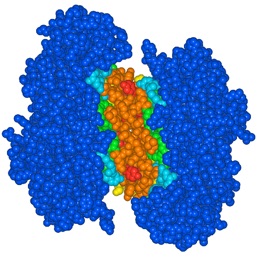
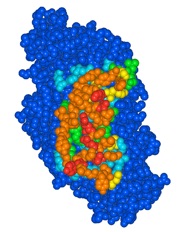
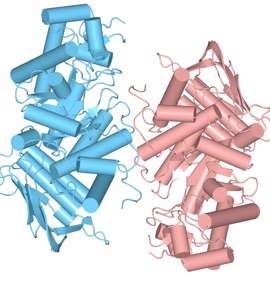
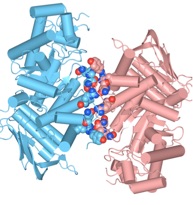
下図はHexosaminidase B(1NOW)で2つのChain間で3.0Å以内の原子を含むアミノ酸残基を抽出した例です。

ダイマーのうちの左側の鎖のみを表示し、90度回転する 接触面がわかりやすくなります。色が赤いほどもう一方のサブユニットに近いことを示します。Contents Info Viewでは、アミノ酸配列上で確認できます。
インタフェースブラウザでもっと詳しく
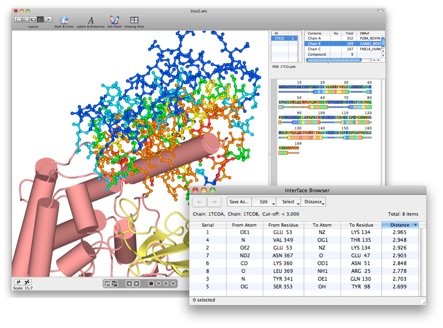
抽出結果は、インタフェースブラウザに表示されます。抽出されたアミノ酸残基や、原子間の距離を表形式で見る事ができます。Workspaceに抽出された構造と照らし合わせれば、どのアミノ酸残基のどの原子が何と結合しているのかをより詳しく調べることができます。
Structure Viewの構造上で抽出された残基間の距離を表示することも可能です。
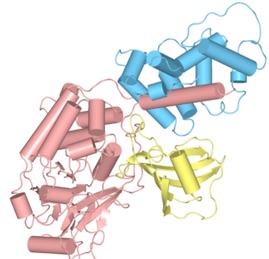
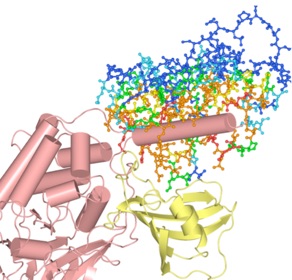
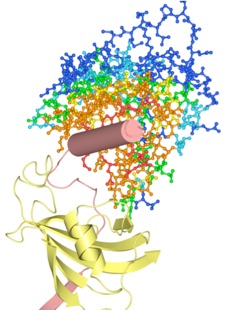
Calcineurin AをCylinder & Strandsで、Calcineurin Bを距離による色分け表示にしています。右図は、Calcineurin AのC末端領域が見やすいように、Chain AのN末端から347残基をHide機能で隠しています。
Calcineurin A (light red), Calcineurin B (light blue),
FKBP12 (light yellow) の複合体
複合体からタンパク質間の相互作用を検出する
PDBには、複数のタンパク質の複合体の構造も登録されています。Chain Interface機能で、複数のタンパク質が会合した時の状態から相互作用するアミノ酸残基を検出することができます。距離による色分け表示では、立体構造上で相互作用するアミノ酸残基の位置を確認できます。インターフェイスブラウザでは、抽出されたアミノ酸残基の原子間の距離が表形式で示されます。下図はCalcineurin A (catalytic subunit), Calcineurin B (regulatory subunit) , FKBP12の複合体(1TCO)のCalcineurin A (Chain A)とCalcineurin B (Chain B) の相互作用を見るために、Chain AとBの間で3.0Å以内にあるアミノ酸残基を抽出した例です。
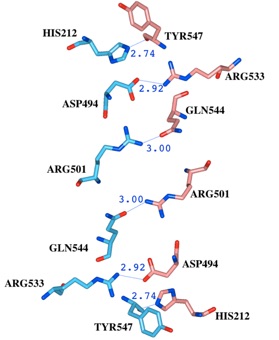
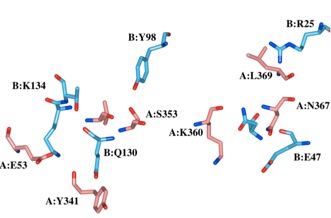
Workspaceに格納された抽出されたアミノ酸残基Calcineurin A
(Chain A)をLight Redで、 Calcineurin B (Chain B)をLight Blueで、
ラベルを付けて表示しています。
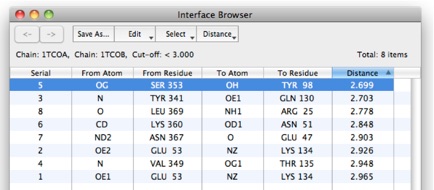
Calcineurin A1TCOのChain AとChain Bの間で3.0Å以内にあるアミノ酸残基をChain Interfaceにより抽出した後のインターフェイスブラウザ。距離で並べ替えています。アミノ酸残基と原子、距離が表形式で表示されます。
Waalsの特長

タンパク質分子のためのインタフェース
見る・調べる
もっと便利に
保存する
動画を作成する
作図する
分子間の距離関係を調べる
重ね合わせと比較

蛋白質のためのインタフェース
Waalsの特長
見る・調べる
作図する
分子間の距離関係を調べる
重ね合わせと比較
もっと便利に
保存する
動画を作成する
Chain Interfaceの使用例として、Hexosaminidase Bで、ダイマーインタフェースを抽出する例を紹介しています。
Copyright © 2009-2013 Altif Laboratories Inc. All rights reserved.